北京权威湿疹医院 http://m.39.net/pf/a_8814564.html
摘自TsiehSun,M.D.(孙捷)著,叶向军译,卢兴国审校《血液肿瘤图谱》(人民军医出版社,)
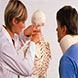
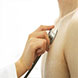
病例资料患者男,71岁。有肺癌脑转移病史。在一次随诊中,发现白细胞数达20.5×/L,原始细胞15%。两周后,患者入院时白细胞数升至62.7×/L,原始细胞81%(图1)。骨髓涂片显示原始单核细胞85%,幼单核细胞7%,单核细胞3%(图2),在髓系和红系细胞中仅剩5%正常造血细胞。骨髓活检显示细胞高增生,大部分正常造血被不成熟单核细胞取代(图3)。
图1外周血涂片可见几个含颗粒的原始单核细胞(Wright-Giemsa×)
图2骨髓涂片显示两个吞噬红细胞的原始细胞(噬血现象),左图箭头指处为吞噬有核红细胞,右图箭头指处为吞噬红细胞(Wright-Giemsa×)
图3骨髓活检显示增生极度活跃,大原始单核细胞增生占优势,箭头指处为原始细胞噬血现象(HE×60)
鉴别诊断急性髓细胞白血病。
进一步检查骨髓流式细胞仪检查:髓过氧化物酶30%,CD13-CD%,CD%,CD11c29%,HLA-DR87%,CD%,CD70%。
细胞化学染色:双重酯酶染色原始细胞α-丁酸萘酯酶阳性,氯乙酸酯酶阴性(图4),髓过氧化物酶染色原始细胞呈阳性。
细胞遗传学核型:t(8;16)(p11.2;p13.3)。
图4骨髓涂片双重酯酶染色显示非特异性酯酶阳性的原始单核细胞(×)
讨论在本病例中,骨髓中单核系细胞占95%,原始单核细胞85%,并经非特异性酯酶染色确证。因此,急性单核细胞白血病的诊断成立。此外,外周血原始单核细胞显示明显的胞质颗粒以及骨髓中发现吞噬红细胞的原始细胞。这些细胞学特征是典型的急性髓细胞白血病(AML)伴t(8;16)(p11;p13)亚型的特征[1]。这种AML亚型非常罕见,大约只有50例新发AML和治疗相关AML病例的报告[2]。大部分病例为单核细胞白血病(M5a或M5b)或粒单细胞白血病(M4)。
M5的临床特征是常有凝血功能紊乱,或者弥漫性血管内凝血(DIC)或者原发纤溶症。次要临床特征是髓外累及并增加了中枢神经系统疾病的风险。在一组29例患者的一系列研究中,41%肝肿大,33%脾肿大,37%淋巴结肿大[3]。其他器官受累,包括皮肤、牙龈、骨骼、中枢神经系统和睾丸。这一疾病预后不良,中位生存期仅两个月[2]。
该亚型的实验室检查包括细胞化学染色和流式细胞免疫表型分析。虽然大多数单核细胞白血病髓过氧化物酶染色呈弱阳性,但是M5伴t(8;16)病例显示髓过氧化物酶或苏丹黑染色强阳性[1]。在M5病例中,非特异性酯酶(α-丁酸萘酯酶)染色阳性,而M4病例中,非特异性和特异性酯酶(氯乙酸酯酶)都呈阳性反应。在M4病例,酯酶双染色经常在同一个白血病细胞中显示两种染色,这种现象描述为过渡型粒单细胞变异[1]。免疫表型上,此亚型表达所有粒单细胞标记,包括CD4、CD11b、CD13、CD14、CD15和CD33[1,4]。HLA-DR的存在,对排除急性早幼粒细胞白血病(M3)特别重要。原始细胞标记如CD34和CD,通常缺乏,或比例低;CD56也经常显示[4]。
分子研究探明MOZ(单核细胞白血病锌指)基因位于8p11断裂点而CBP(CREB结合蛋白)基因位于16q13断裂点[1,2]。作为易位的结果,这两个基因的融合产物(蛋白),可能会通过三种机制导致白血病的发生:(1)融合产物错误地靶向错误基因,而不是这两个独立蛋白质本来靶向的基因;(2)融合产物错误调节目标基因;(3)融合产物失去指导DNA转录的正常功能[5]。白血病产生的其他机制包括因特异性组蛋白乙酰转移酶(HAT)活性错误靶向而致染色质异常乙酰化,和对RUNX1介导的转录的抑制[2]。
识别这一罕见AML亚型的重要性是因为它的不良预后和与其他恶性病程的相似性。由于在M3颗粒过少变异型中出现有颗粒单核系细胞,t(8;16)AML可能会被误诊为急性早幼粒细胞白血病,特别是两者都会出现凝血功能紊乱的特点。HLA-DR的存在可能有助于排除M3,但分子遗传学检查是它们区别的关键。肿瘤细胞出现吞噬红细胞现象还可导致误诊为恶性组织细胞增多症或T细胞肿瘤。
参考文献1.SunT,WuE.Acutemonoblasticleukemiawitht(8;16):Adistinctclinicopathologicentity;Reportofacaseandreviewoftheliterature.AmJHematol;66;–.
2.RozmanM,CamosM,ColomerD,etal.Type1MOZ/CBP(MYST3/CREBBP)isthemost



 当前时间:
当前时间:  E-Mail:
E-Mail: